 |
| Etude sur la protéine MSH3 dans le cadre de la maladie de Huntington Le gène MSH3 est utile pour réparer notre ADN mais dans le cadre de la M.H, il peut cafouiller. |
Un gène appelé MSH3 est utile pour réparer notre ADN mais dans le cadre de la maladie de Huntington, il peut cafouiller et provoquer des allongements des répétitions CAG. Les chercheurs ont découvert de nouvelles informations s’agissant de la manière dont l’activité du gène MSH3 est contrôlée, ouvrant la porte à de nouvelles pistes thérapeutiques.
Ce gène, lequel code une protéine impliquée dans la réparation et la maintenance de notre ADN, est devenu un sujet brûlant dans la recherche MH depuis qu’il est impliqué par de multiples études génétiques comme facteur clé dans la maladie. Aux termes d’une récente publication, une équipe de scientifiques de l’Université Nationale d’Irlande (Galway) a fournit des informations sur la manière dont la protéine MSH3 est contrôlée dans nos cellules, ce qui pourrait être utile pour concevoir des médicaments visant à ralentir ou même empêcher la MH.
![]() MSH3 - L'épée à double tranchant
MSH3 - L'épée à double tranchant
La molécule protéique MSH3 agit en corrigeant les erreurs génétiques et en protégeant nos génomes contre l’assaut continu des dommages à l’ADN auxquels ils sont confrontés au quotidien. Pour ce faire, elle scanne notre ADN, recherchant des erreurs et recrutant d’autres protéines pour l’aider à les réparer lors d’un processus appelé ‘réparation des mésappariements’.
Comme vous le savez peut-être, la maladie de Huntington est provoquée par une séquence inhabituellement longue de bases d’ADN répétitives, ‘C’-‘A’-‘G’ (les éléments constitutifs du code génétique), au sein d’un gène appelé ‘huntingtin’. Dans les zones cérébrales affectées par la MH, cette expansion de triplets ADN est ‘instable’ – ce qui signifie que davantage d’unités répétitives pourraient être ajoutées tout au long de la vie. On appelle ce processus ‘l’expansion de triplets ADN’ ou instabilité somatique. Dans la plupart des maladies à expansion de triplets, comme la MH, plus la taille de l’expansion augmente, plus les symptômes de la maladie s’aggravent.
Lorsque la protéine MSH3 rencontre cette répétition CAG dans notre ADN, elle reconnaît qu’il s’agit d’une erreur et essaie de la réparer mais elle introduit en fait encore davantage de répétitions, ce qui aggrave encore les choses.
![]() Alors, comment peut-on empêcher cela ?
Alors, comment peut-on empêcher cela ?
Si on pouvait concevoir un médicament empêchant la protéine MSH3 de commettre cette erreur, on pourrait ralentir ou empêcher le processus d’expansion de triplets, ce qui, on l’espère, pourrait ralentir la maladie, ou même l’arrêter complètement dans son élan... Mais comment peut-on réaliser cela sans perturber la fonction normale de la protéine MSH3, celle de protéger notre code génétique ? Normalement, en l’absence de gènes de réparation de l’ADN, toutes sortes de problèmes peuvent survenir du fait de l’accumulation de dommages à l’ADN, tels que le cancer par exemple. Ce qui est très intéressant s’agissant de la protéine MSH3, c’est que, contrairement à d’autres protéines de réparation de l’ADN connues pour être impliquées dans le processus d’expansion de triplets, la suppression complète de celle-ci ne semble pas avoir beaucoup d’effets secondaires négatifs.
![]() Alors, quoi de neuf ?
Alors, quoi de neuf ?
Nos cellules peuvent ralentir le travail de la protéine MSH3 en ajoutant une signature chimique appelée un groupe acétyle, et l’accélérer en supprimant le groupe acétyle. Dans la mesure où le travail plus rapide de la protéine MSH3 signifierait une expansion de triplets ADN plus rapide, les scientifiques veulent empêcher l'effacement de cette marque d'acétyle. De précédentes études suggèrent qu’une protéine appelée HDAC3 est impliquée dans le processus d’élimination. Le laboratoire Laheu de l’Université Nationale d’Irlande (Galway) a testé un médicament dans des cellules humaines qui empêche la protéine HDAC3 de fonctionner normalement, et a examiné ses effets sur l’expansion de triplets ADN.
![]() Qu'ont constaté les chercheurs ?
Qu'ont constaté les chercheurs ?
Les chercheurs ont constaté que le médicament interrompait les expansions de triplets ADN dans les cellules humaines, et, plus important, que celui-ci n’affectait pas d’autres activités importantes de la réparation de l’ADN, suggérant que cette thérapie ne se ferait pas au prix d'un risque accru de cancer.
Ils ont également utilisé ce médicament pour mieux comprendre la manière dont la protéine HDAC3 contrôle l’activité de la protéine MSH3. Les molécules protéiques possèdent des signaux spéciaux appelés ‘signaux de localisation nucléaire’ (‘NSL’ en abrégé) qui agissent comme un code postal dirigeant les protéines vers le noyau où notre ADN est conservé. Les chercheurs se sont rendu compte que la marque acétyle modifiait le 'code postal' de la protéine MSH3, dirigeant celle-ci hors du noyau où elle ne pouvait plus entraîner de longues expansions de triplets ADN.
![]() Alors, qu'est-ce que tout cela signifie ?
Alors, qu'est-ce que tout cela signifie ?
Globalement, leur étude suggère un nouveau mécanisme de régulation pour les expansions de triplets de l’ADN grâce à l’élimination des groupes acétyles de la protéine MSH3 par la protéine HDAC3. Cela peut expliquer pourquoi des patients ayant certaines versions de la protéine MSH3 présentent une évolution plus lente de la maladie, si, par exemple, leur groupe acétyle est plus difficile à éliminer.
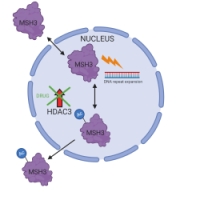
Comment le médicament réduit-il l’expansion de triplets ADN ?
Lorsqu’un groupe Acétyl (Ac) est ajouté à la protéine MSH3, celle-ci est dirigée hors du noyau où elle ne peut accéder à la répétition CAG – arrêtant ainsi l’expansion de triplets.
La protéine HDAC3 élimine normalement ce groupe acétyl (Ac), permettant à la protéine MSH3 de rester dans le noyau et de conduire à des expansions.
Lorsque les scientifiques traitent les cellules avec ce médicament, la protéine HDAC3 n’est plus en mesure d’effacer la marque acétyle, ce qui signifie que la protéine MSH3 reste coincée à l’extérieur du noyau où elle ne peut accéder à la répétition CAG (schéma réalisé avec BioRender).
Comprendre les mécanismes de la maladie de cette manière ouvre des portes pour la conception de médicaments visant à ralentir le processus d’expansion de triplets ADN (et par conséquent, la maladie elle-même) – d’autant plus que les chercheurs prétendent que l’inhibition de la protéine MSH3 n’affecte pas la fonction de base de la réparation des mésappariements d'ADN. Le médicament utilisé dans cette étude est puissant, sélectif et assez bien étudié ; il peut donc déjà être un candidat clinique prometteur en soi.
Cela dit, jouer avec les protéines HDAC peut avoir toutes sortes d’autres effets indésirables dans les cellules.
Il sera nécessaire de s’assurer que les médicaments ciblant la protéine HDAC3 sont sans danger avec des effets secondaires limités. De plus, il sera nécessaire de trouver un moyen d’administrer l’inhibiteur de la protéine HDAC3 aux régions profondes du cerveau qui sont affectées par la MH, ce qui a tendance à être assez difficile.
En résumé, les travaux des chercheurs se montrent prometteurs mais il reste encore beaucoup à faire avant de pouvoir nous enthousiasmer s’agissant de cette thérapie potentielle.
Traduction Libre (Dominique C . - Michelle D.)